Mukoviszidose-Forschung: Können die Zellen der Lunge durch eine mRNA-Therapie den CFTR-Kanal ausreichend selbst herstellen?
Es gibt immer noch Menschen mit Mukoviszidose, für die eine Therapie mit Modulatoren nicht möglich ist. Entweder, weil sie seltene CFTR-Varianten haben, bei denen die Modulatoren nicht wirken können oder weil sie die Modulatoren nicht vertragen.
Vorarbeiten für das aktuelle Forschungsprojekt wurden bereits erfolgreich abgeschlossen und publiziert („Self-assembled peptide-poloxamine nanoparticles enable in vitro and in vivo genome restoration for cystic fibrosis“: DOI: 10.1038/s41565-018-0358-x. Epub 2019 Jan 28). Hierfür ist Joseph Rosenecker 2021 der Adolf-Windorfer-Preis vom Mukoviszidose e.V. überreicht worden.
Vektoren beeinflussen Verträglichkeit und Effektivität der genbasierten Therapie
Ein vielversprechender Ansatz für die Behandlung von CF-Lungenerkrankungen könnte eine Inhalation von im Labor hergestellter CFTR-mRNA sein. Die CFTR-mRNA soll dabei der Zelle die Anleitung bieten, den CFTR-Kanal selbst herzustellen. Jüngste klinische Studien, welche die Anwendung von IVT-CFTR-mRNA in der Lunge von Patientinnen und Patienten mit Mukoviszidose untersuchten, zeigten jedoch nur eine begrenzte klinische Wirksamkeit. Die Forschenden führten dies auf einen nicht ausreichenden Transport der CFTR-mRNA in die Zielzellen der Atemwege und des Lungenparenchyms zurück. Zudem zeigten sich nach der Applikation Nebenwirkungen.
Die Verträglichkeit und Effektivität der Therapie mit CFTR-mRNA hängt entscheidend von den Vektoren ab, welche die mRNA zu den Zellen bringen. Die Arbeitsgruppe um Prof. Josef Rosenecker vom Dr. von Haunerschen Kinderspital des LMU Klinikums hat bereits eine neuartige Klasse von mRNA-Vektoren auf Basis von Poloxamin-Lipid-Nanopartikeln (PolixNano) entwickelt, die eine effiziente Zufuhr von CFTR-mRNA zu den Atemwegen ermöglicht. Ebenso entwickelten die Forschenden eine leicht veränderte CFTR-mRNA, um die Herstellung des Proteins anhand dieser Vorlage zu verbessern.
Bilden Lungenzellen CFTR-Protein nach Vernebelung von CFTR-mRNA PolixNano?
Die aktuelle Forschungsarbeit soll diesen Ansatz nun weiter in Richtung klinische Anwendung prüfen. Im Fokus stehen dabei Laboruntersuchungen, um die Effektivität, mit der die mRNA in die Zellen gelangt und dort zur Herstellung von Protein führt, zu messen. Das erfolgt zunächst in vitro in einem Zellmodell, anschließend auch in-vivo durch Verneblung in einem Tiermodell. Zur Beurteilung der Effektivität wird neben der CFTR-mRNA auch ein Reportergen verwendet, also die mRNA eines Gens, mit dessen Hilfe die Effektivität der Proteinherstellung beispielhaft und leicht nachweisbar verfolgt werden kann. Diese Experimente sollen zeigen, ob körpereigene Zellen den CFTR-Kanal durch Inhalation von CFTR-mRNA PolixNano in ausreichender Menge selber herstellen können.
mRNA-Therapien bereits für andere Erkrankungen zugelassen

„Eine mRNA-Therapie bei Mukoviszidose wäre sogar mutationsunabhängig und könnte allen Menschen mit Mukoviszidose helfen“, erläutert Prof. Josef Rosenecker von der Kinderklinik im Dr. von Haunerschen Kinderspital am LMU Klinikum. „Eine Verabreichung per Inhalation bietet allerdings zunächst nur eine Therapie für die Lungenerkrankung bei CF an. Andere Organe müssten auf anderen Wegen erreicht werden. Und eine CFTR-mRNA Inhalation wirkt auch nur vorübergehend, da die mRNA im Körper nach einiger Zeit abgebaut wird und daher erneut eingebracht werden muss.“ Derzeit ist diese mögliche Therapieoption noch in der präklinischen Entwicklung. Eine klinische Anwendung ist daher zeitnah nicht zu erwarten. Es werden aber voraussichtlich schon bald Zulassungen für mRNA-Therapien bei anderen Erkrankungen erfolgen.
Forschungsförderung
Mit seiner Forschungsförderung unterstützt der Bundesverband Mukoviszidose e.V. ein breites Spektrum an Projekten von medizinischer Grundlagenforschung bis zu klinischen Studien, um Therapieoptionen und Lebensqualität für Betroffene zu verbessern. Weitere Informationen zur Forschungsförderung des Mukoviszidose e.V.
Über den Bundesverband Mukoviszidose e.V.
Der Bundesverband Mukoviszidose e.V. vernetzt die Patienten, ihre Angehörigen, Ärzte, Therapeuten und Forscher. Er bündelt unterschiedliche Erfahrungen, Kompetenzen sowie Perspektiven mit dem Ziel, jedem Betroffenen ein möglichst selbstbestimmtes Leben mit Mukoviszidose zu ermöglichen. Um die vielfältigen Aufgaben und Ziele zu erreichen, ist die gemeinnützige Patientenorganisation auf die Unterstützung engagierter Spender und Förderer angewiesen.
FAQ – die wichtigsten Fragen und Antworten zu Mukoviszidose
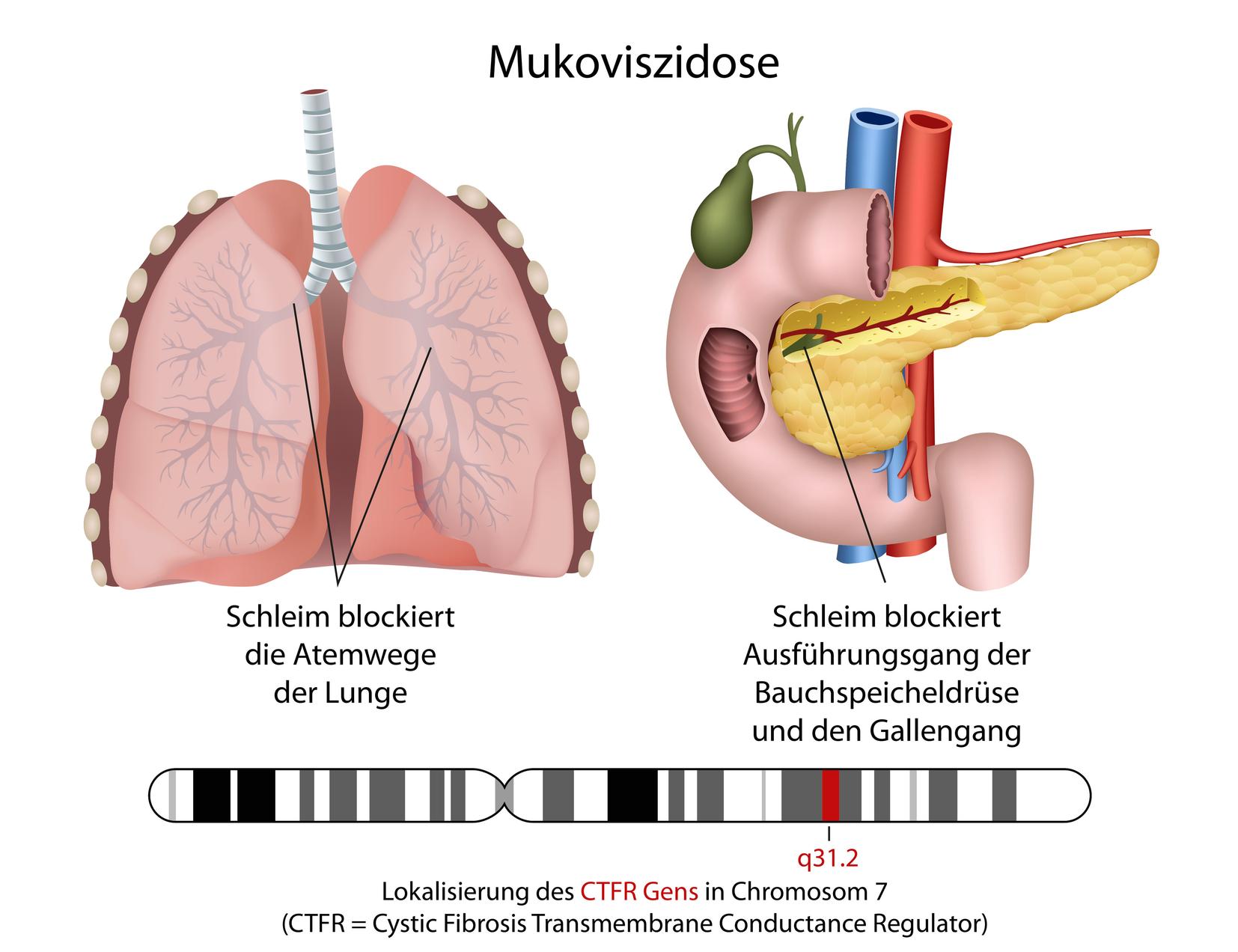
In Deutschland sind mehr als 8.000 Kinder, Jugendliche und Erwachsene von der unheilbaren Erbkrankheit Mukoviszidose betroffen. Durch eine Störung des Salz- und Wasserhaushalts im Körper bildet sich bei Mukoviszidose-Betroffenen ein zähflüssiges Sekret, das Organe wie die Lunge und die Bauchspeicheldrüse irreparabel schädigt. Jedes Jahr werden in Deutschland etwa 150 bis 200 Kinder mit der seltenen Krankheit geboren.
CFTR-Modulatoren sind Arzneistoffe, die spezifisch das defekte CFTR-Protein aktivieren um dessen Funktion als Salzkanal zu verbessern. Dadurch normalisiert sich der Salz- und Wasserhaushalt der betroffenen Organe und die für Mukoviszidose typischen Beschwerden werden gelindert oder verschwinden vollständig.
Die pulmonalen Symptome der Mukoviszidose, wie die vermehrte Bildung von zähflüssigen Atemwegsekreten und in deren Folge die Häufung bakterieller Infektionen der Atemwege, werden durch die Therapie mit Modulatoren deutlich weniger. Dadurch verbessert sich die Lungenfunktion und es kommt zu weniger Atemwegsinfektionen. CFTR-Modulatoren haben als Langzeittherapie die Prognose und die Lebensqualität für viele der betroffenen CF-Patienten deutlich verbessert.
Trotz der Fortschritte durch CFTR-Modulatoren können aktuell schätzungsweise rund 10 Prozent der Mukoviszidose-Patienten nicht mit diesen Therapien behandelt werden, da einige Patienten Mutationen haben, auf die die derzeitigen Modulatoren nicht ansprechen. Andere Patienten können die Medikamente wegen der Nebenwirkungen nicht einnehmen. Für diese Patientengruppen könnte die CFTR-mRNA-Therapie eine mögliche Option sein. Denn die CFTR-mRNA-Therapie kann unabhängig von der zugrundeliegenden Mutation angewendet werden. Es wird im Gegensatz zu der Modulatortherapie das CFTR-Protein von den körpereigenen Zellen gebildet. Die CFTR-mRNA, die über die Atemwege in die Lunge verabreicht wird, dient lediglich als Anleitung für die Bildung eines funktionsfähigen CFTR-Proteins.
Kontakt
Prof. Dr. med. Rosenecker, Josef
Kinderklinik und Kinderpoliklinik im Dr. von Haunerschen Kinderspital, LMU Klinikum München

